question ED espèces et diagramme
3 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE GENERALE
Page 1 sur 1
 Re: question ED espèces et diagramme
Re: question ED espèces et diagramme
Salut !
Sur un diagramme de pourbaix, tu représentes à la fois des couples ox/réd et des couples acide/base :
- Sur l'axe des abscisses, tu lis le pH, donc plus tu vas vers la droite, plus le pH est élevé, plus tu vas vers la gauche et plus il est bas.
Ainsi, tu placeras ton acide plutôt vers la gauche (pH bas) de ton diagramme, et ta base plutôt vers la droite (pH élevé).
- Sur l'axe des ordonnées, tu lis le potentiel, donc plus tu montes, plus le potentiel est élevé, plus tu descends et plus il est bas.
Ainsi, tu placeras ton oxydant vers le haut, et ton réducteur vers le bas.
Ici, tu as 4 zones : A, B, C & D
Les zones A et D sont plutôt liées au pH : elles sont séparées par une courbe verticale (donc à partir d'un certain pH, on passe de A à D.
Les zones B & C sont plutôt liées au potentiel : elles sont séparées par une courbe horizontale (donc à partir d'un certain potentiel, on passe de C à B).
Donc sur toutes les espèces on a :
A = acide
B = oxydant
C = réducteur
D = base
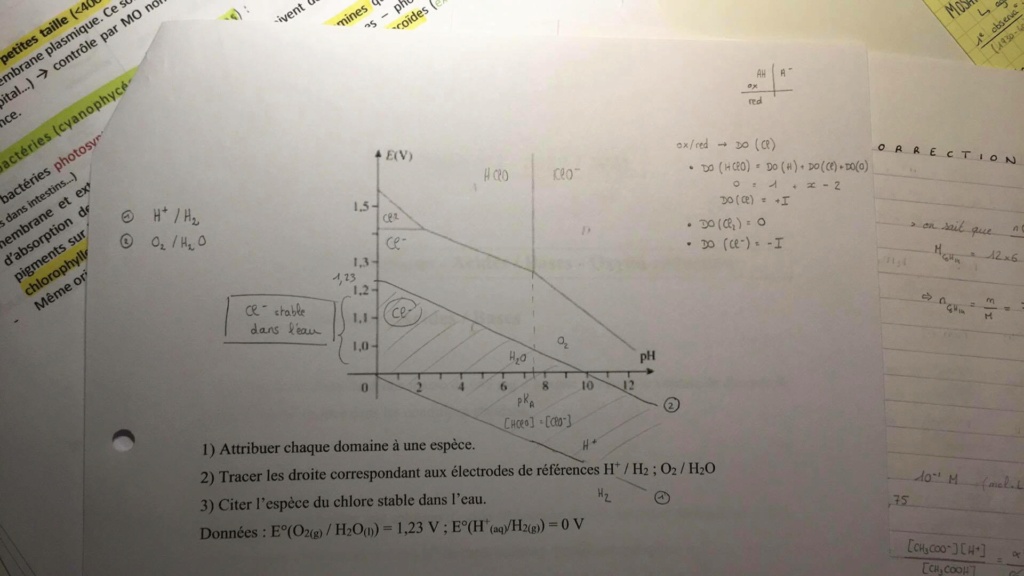
On te donne HClO, Cl2, Cl- et ClO-
Une espèce acide est une espèce capable de céder un proton, l'espèce acide est celle qui possède un H, donc HClO
Ainsi HClO -> ClO- + H+, donc la base conjuguée est ClO-
Il nous reste donc Cl- et Cl2 : un oxydant est capable de capter des électrons, un réducteur est capable d'en céder : Cl- peut céder des électrons (il a une charge négative) donc il est réducteur et Cl2 est capable d'en capter donc oxydant
Au final on a donc :
A = acide = HClO
B = oxydant = Cl2
C = réducteur = Cl-
D = base = ClO-
Est-ce que c'est ok pour toi ?
Sur un diagramme de pourbaix, tu représentes à la fois des couples ox/réd et des couples acide/base :
- Sur l'axe des abscisses, tu lis le pH, donc plus tu vas vers la droite, plus le pH est élevé, plus tu vas vers la gauche et plus il est bas.
Ainsi, tu placeras ton acide plutôt vers la gauche (pH bas) de ton diagramme, et ta base plutôt vers la droite (pH élevé).
- Sur l'axe des ordonnées, tu lis le potentiel, donc plus tu montes, plus le potentiel est élevé, plus tu descends et plus il est bas.
Ainsi, tu placeras ton oxydant vers le haut, et ton réducteur vers le bas.
Ici, tu as 4 zones : A, B, C & D
Les zones A et D sont plutôt liées au pH : elles sont séparées par une courbe verticale (donc à partir d'un certain pH, on passe de A à D.
Les zones B & C sont plutôt liées au potentiel : elles sont séparées par une courbe horizontale (donc à partir d'un certain potentiel, on passe de C à B).
Donc sur toutes les espèces on a :
A = acide
B = oxydant
C = réducteur
D = base
On te donne HClO, Cl2, Cl- et ClO-
Une espèce acide est une espèce capable de céder un proton, l'espèce acide est celle qui possède un H, donc HClO
Ainsi HClO -> ClO- + H+, donc la base conjuguée est ClO-
Il nous reste donc Cl- et Cl2 : un oxydant est capable de capter des électrons, un réducteur est capable d'en céder : Cl- peut céder des électrons (il a une charge négative) donc il est réducteur et Cl2 est capable d'en capter donc oxydant
Au final on a donc :
A = acide = HClO
B = oxydant = Cl2
C = réducteur = Cl-
D = base = ClO-
Est-ce que c'est ok pour toi ?

Asticoo- Messages : 589
Date d'inscription : 22/09/2017
Petiot aime ce message
 Re: question ED espèces et diagramme
Re: question ED espèces et diagramme
Oui c'est très clair, merci beaucoup !! 
etoile- Messages : 2
Date d'inscription : 10/11/2020
 Re: question ED espèces et diagramme
Re: question ED espèces et diagramme
Salut,
Concernant H+/H2 et O2/H2O, pourquoi sont-ils en bas ? Est-ce en rapport avec le fait que l'eau a une pente négatif quand elle change d'état ?
Concernant H+/H2 et O2/H2O, pourquoi sont-ils en bas ? Est-ce en rapport avec le fait que l'eau a une pente négatif quand elle change d'état ?
Fafa- Messages : 70
Date d'inscription : 24/11/2019
 Re: question ED espèces et diagramme
Re: question ED espèces et diagramme
Pour placer les couples H+/H2 et O2/H2O, on détermine dans un premier temps le potentiel E de chaque couple, en faisant intervenir le pH, ce qui donne une équation de droite affine, que tu peux représenter sur ton diagramme !
Elles sont toujours identiques, puisqu'elles dépendent de E°, le potentiel standard, qui ne varie pas
Ensuite, tu places chaque espèce dans sont domaine : pour le couple H+/H2, H+ est l'oxydant, il sera donc au-dessus de la droite représentant le couple et H2 est le réducteur, il sera donc en-dessous de cette droite.
Idem pour O2/H2O : O2 est oxydant donc au-dessus de la droite du couple, H2O réducteur donc en-dessous.
Entre les deux droites se trouve donc le domaine de l'eau (H2O).
Si ta question faisait référence à l'inclinaison des droites, ça vient tout simplement de leur équation de droite, donc de l'équation de Nerst
J'espère que ça répond à ta question
Elles sont toujours identiques, puisqu'elles dépendent de E°, le potentiel standard, qui ne varie pas
Ensuite, tu places chaque espèce dans sont domaine : pour le couple H+/H2, H+ est l'oxydant, il sera donc au-dessus de la droite représentant le couple et H2 est le réducteur, il sera donc en-dessous de cette droite.
Idem pour O2/H2O : O2 est oxydant donc au-dessus de la droite du couple, H2O réducteur donc en-dessous.
Entre les deux droites se trouve donc le domaine de l'eau (H2O).
Si ta question faisait référence à l'inclinaison des droites, ça vient tout simplement de leur équation de droite, donc de l'équation de Nerst
J'espère que ça répond à ta question

Asticoo- Messages : 589
Date d'inscription : 22/09/2017
 Re: question ED espèces et diagramme
Re: question ED espèces et diagramme
Oui tu as répondu à ma question. Merci beaucoup
Fafa- Messages : 70
Date d'inscription : 24/11/2019
Asticoo aime ce message
 Sujets similaires
Sujets similaires» Diagramme HF
» Diagramme d'OM
» Diagramme PT eau
» diagramme X
» TK1 2013 Ordre de liaison et carbone 12.
» Diagramme d'OM
» Diagramme PT eau
» diagramme X
» TK1 2013 Ordre de liaison et carbone 12.
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE GENERALE
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|