hybridation azote
3 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
 hybridation azote
hybridation azote
salut !
j'ai vu que dans la molécule H2C=CH-NH2, l'azote était hybridé sp2 et non sp3 en raison du système conjugué, est-ce pareil pour la molécule ci-dessous ? (l'azote serait alors sp et non sp2)
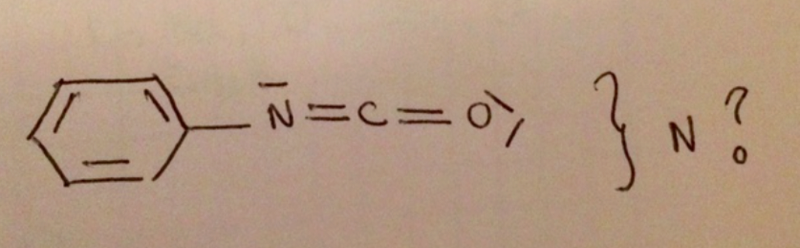
et sinon, dans la molécule de NH3, l'azote est-il hybridé ?
j'ai l'impression que non car sans être hybridé, l'azote étant 1S2, 2S2, 2P3 il peut établir 3 liaisons avec un doublet non liant ce qui est bien le cas dans NH3, il n'aura donc pas besoin d'hybridation, est-ce bien ça ?
j'ai vu que dans la molécule H2C=CH-NH2, l'azote était hybridé sp2 et non sp3 en raison du système conjugué, est-ce pareil pour la molécule ci-dessous ? (l'azote serait alors sp et non sp2)
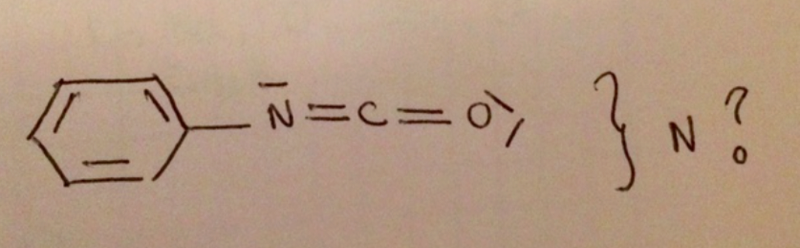
et sinon, dans la molécule de NH3, l'azote est-il hybridé ?
j'ai l'impression que non car sans être hybridé, l'azote étant 1S2, 2S2, 2P3 il peut établir 3 liaisons avec un doublet non liant ce qui est bien le cas dans NH3, il n'aura donc pas besoin d'hybridation, est-ce bien ça ?
Gabrielle.G- Messages : 179
Date d'inscription : 15/10/2017
 Re: hybridation azote
Re: hybridation azote
Salut,
alors pour ton exemple l'azote est effectivement hybridé sp à cause de l'effet mésomère, son doublet non-liant ne lui appartient pas spécifiquement car il est mobile le long de la molécule.
Dans la molécule NH3 l'azote est hybridé sp3, l'hybridation ne détermine pas seulement le nombre de liaison que l'atome peut faire mais également sa structure dans l'espace. Quand on dit que l'azote est hybridé sp3 c'est qu'il forme 4 liaisons et dans la règle VSEPR cela revient à dire qu'il est A4. Le NH3 est A4X3E1 il a donc une forme pyramidale qui lui est permise par son hybridation.
alors pour ton exemple l'azote est effectivement hybridé sp à cause de l'effet mésomère, son doublet non-liant ne lui appartient pas spécifiquement car il est mobile le long de la molécule.
Dans la molécule NH3 l'azote est hybridé sp3, l'hybridation ne détermine pas seulement le nombre de liaison que l'atome peut faire mais également sa structure dans l'espace. Quand on dit que l'azote est hybridé sp3 c'est qu'il forme 4 liaisons et dans la règle VSEPR cela revient à dire qu'il est A4. Le NH3 est A4X3E1 il a donc une forme pyramidale qui lui est permise par son hybridation.
Lenouch- Messages : 136
Date d'inscription : 07/02/2017
Age : 25
 Re: hybridation azote
Re: hybridation azote
Ah ok, merci beaucoup ! 
Gabrielle.G- Messages : 179
Date d'inscription : 15/10/2017
 Re: hybridation azote
Re: hybridation azote
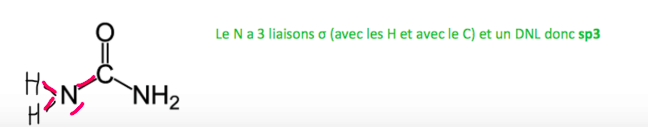
En fait je pensais avoir compris mais j'ai revu ce que j'avais fais en Tuto et je suis tombé sur un exemple que je n'ai pas compris ...selon ce qu'on a dis précédemment, l'azote étant ici encore une fois dans un système conjugué, ne devrait-il pas être sp2 ? (il serait au centre d'un triangle (donc plan) et non pas d'un tétraèdre ?)

Gabrielle.G- Messages : 179
Date d'inscription : 15/10/2017
 Re: hybridation azote
Re: hybridation azote
Coucou,
Il s'agit de mon tuto.
En fait monsieur Boury et monsieur Gautret n'ont pas la même façon de répondre.
En effet en chimie organique il faut regarder si tu es dans un système conjugué dans ce cas ce serait bien sp2.
Mais j'ai demandé tout à l'heure à M. Boury et il m'a repondu : chaque hybride de résonnance à une hybridation différente. En gros sur cette représentation le N serait bien sp3 mais dans une autre forme (par exemple en basculant le doublet non liant sur la liaison avec le C et la double liaison C=O sur le O) il serait sp2.
Je suis vraiment désolée car c'est galère. Ce que je te conseille le jour du concours c'est de bien regardé qui pose la question (normalement il y a écrit chimie organique, structurale etc) et si c'est M. Boury qui pose la question tu te base uniquement sur la molécule que tu as sous les yeux et tu compte les DNL et liaisons sigma.
Je lui ai aussi demander pour le NH3 il m'a dit qu'il était bien hybridé sp3.
Il s'agit de mon tuto.
En fait monsieur Boury et monsieur Gautret n'ont pas la même façon de répondre.
En effet en chimie organique il faut regarder si tu es dans un système conjugué dans ce cas ce serait bien sp2.
Mais j'ai demandé tout à l'heure à M. Boury et il m'a repondu : chaque hybride de résonnance à une hybridation différente. En gros sur cette représentation le N serait bien sp3 mais dans une autre forme (par exemple en basculant le doublet non liant sur la liaison avec le C et la double liaison C=O sur le O) il serait sp2.
Je suis vraiment désolée car c'est galère. Ce que je te conseille le jour du concours c'est de bien regardé qui pose la question (normalement il y a écrit chimie organique, structurale etc) et si c'est M. Boury qui pose la question tu te base uniquement sur la molécule que tu as sous les yeux et tu compte les DNL et liaisons sigma.
Je lui ai aussi demander pour le NH3 il m'a dit qu'il était bien hybridé sp3.

La Gueuse- Messages : 293
Date d'inscription : 07/12/2014
 Re: hybridation azote
Re: hybridation azote
Super merci beaucoup !!
Gabrielle.G- Messages : 179
Date d'inscription : 15/10/2017
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum