QCM 28 TK2
2 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des Talc-Khôlles (TK) et des tutorats :: CHIMIE GENERALE :: TK & Tutos 2015-2016
Page 1 sur 1
 QCM 28 TK2
QCM 28 TK2
Bonjour,
Je n'arrive pas à comprendre comment on trouve que la réponse B est bonne dans cette exercice :

Car si on fait le diagramme de Hess on obtient :
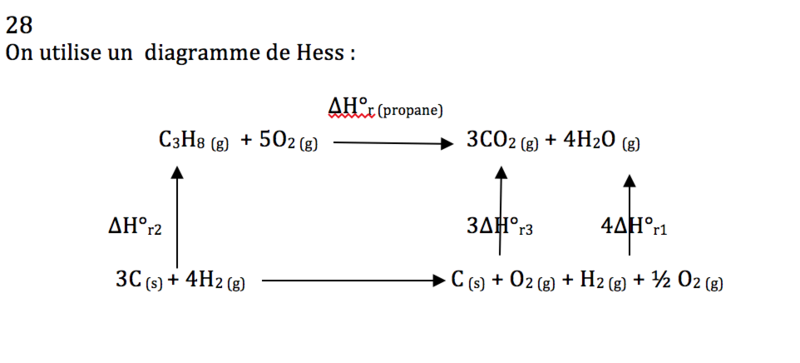
Et du coup après si j'applique la formule
DeltaH°r = Somme produits - Somme réactifs ; j'obtiens :
Delta H°r = 3deltaH°R3 + 4deltaH°r1 - deltaH°R2
Mais je ne parviens pas a trouver comment on obtient le -4deltaH°R1 ...
Pourriez vous m'indiquer quelle est mon erreur ?
Merci d'avance
Je n'arrive pas à comprendre comment on trouve que la réponse B est bonne dans cette exercice :

Car si on fait le diagramme de Hess on obtient :

Et du coup après si j'applique la formule
DeltaH°r = Somme produits - Somme réactifs ; j'obtiens :
Delta H°r = 3deltaH°R3 + 4deltaH°r1 - deltaH°R2
Mais je ne parviens pas a trouver comment on obtient le -4deltaH°R1 ...
Pourriez vous m'indiquer quelle est mon erreur ?
Merci d'avance
V.Dsw- Messages : 91
Date d'inscription : 10/09/2016
 Re: QCM 28 TK2
Re: QCM 28 TK2
Coucou,
C'est parce que ici le deltaH R1 correspond au passage de H2O à H2 + O2 or dans ton diagramme de Hess la flèche part des corps simple vers H2O donc tu dois mettre -DeltaH R1.
C'est plus clair ?
C'est parce que ici le deltaH R1 correspond au passage de H2O à H2 + O2 or dans ton diagramme de Hess la flèche part des corps simple vers H2O donc tu dois mettre -DeltaH R1.
C'est plus clair ?

La Gueuse- Messages : 293
Date d'inscription : 07/12/2014
 QCM 28 TK2
QCM 28 TK2
Salut,
Désolé d'insister, je comprend bien qu'il faut mettre un "-" car on considère de l'énergie de liaison et non plus de dissociation c'est bien ça ?
Mais ce que je continue à ne pas comprendre c'est pourquoi dans ce cas on mettrait pas un "-" devant delta H°R2 et delta H°R3 du coup ?
Désolé d'insister, je comprend bien qu'il faut mettre un "-" car on considère de l'énergie de liaison et non plus de dissociation c'est bien ça ?
Mais ce que je continue à ne pas comprendre c'est pourquoi dans ce cas on mettrait pas un "-" devant delta H°R2 et delta H°R3 du coup ?
V.Dsw- Messages : 91
Date d'inscription : 10/09/2016
 Re: QCM 28 TK2
Re: QCM 28 TK2
Attention ici il n s'agit pas d'enthalpie de liaison ou de dissociation, si tu regardes bien les enthalpies de réaction R1 2 3 qui te sont données sont en fait les enthalpies standard de formation du propane, du CO2 et l'eau.
Dans ton diagramme de Hess il faut que tu mette les flèche dans le sens des réaction qu'on te donne.
* R1 : c'est le passage de H2O à H2 + O2 (c'est donc l'inverse de l'enthalpie de formation)
* R2 : c'est l'enthalpie de formation du propane : c'est le passage du H2 et C à C3H8
* R3: c'est l'enthalpie de formation du CO2 : passage de C + O2 à CO2
Dans ton diagramme de Hess ta fleche pour R1 est à l'envers. Si tu gardes deltaH R1 il faut que ta flèche soit dans l'autre sens, si tu la laisse dans ce sens la il faut que tu mettes -deltaHR1.
Ensuite une fois que tu as fait ton diagramme on écrit la formule: je vais me baser sur le diagramme que tu as fait.
DeltaH réaction du propane = -deltaH R2 (car R2 ne va pas dans le sens de la réaction) + DeltaH R3 (R3 va bien dans le sens de la réaction c'est bon) + (-DeltaH R1) (la flèche va dans le sens de la réaction mais comme je l'ai dit plus haut si la flèche est dans ce sens c'est -R1).
Quant tu fais ton diagramme de Hess tu as deux possibilités:
* soit tu met toutes tes fleches allant vers le produit de la réaction (donc celle de gauche qui descend et celle de droite qui remonte): dans ce cas il faut que tu fasse en notant à coté au signe de tes enthalpies. Mais quand tu passe au calcul tu n'a plus qu'à faire l'enthalpie de réaction = la somme des enthalpies de ton autre chemin (car toutes tes flèches seront dans le bon sens)
* soit tu met les flèches dans le sens des enthalpies qu'on te donne dans l'énoncé donc tu n'as pas de changement de signe à faire sur ton diagramme. Mais attention au moment de passer au calcul il faut bien que tu aille dans le sens de la réaction (ici vers la formation de CO2 et H2O qui sont les produit de la réaction du propane).
Tu as compris ?
Dans ton diagramme de Hess il faut que tu mette les flèche dans le sens des réaction qu'on te donne.
* R1 : c'est le passage de H2O à H2 + O2 (c'est donc l'inverse de l'enthalpie de formation)
* R2 : c'est l'enthalpie de formation du propane : c'est le passage du H2 et C à C3H8
* R3: c'est l'enthalpie de formation du CO2 : passage de C + O2 à CO2
Dans ton diagramme de Hess ta fleche pour R1 est à l'envers. Si tu gardes deltaH R1 il faut que ta flèche soit dans l'autre sens, si tu la laisse dans ce sens la il faut que tu mettes -deltaHR1.
Ensuite une fois que tu as fait ton diagramme on écrit la formule: je vais me baser sur le diagramme que tu as fait.
DeltaH réaction du propane = -deltaH R2 (car R2 ne va pas dans le sens de la réaction) + DeltaH R3 (R3 va bien dans le sens de la réaction c'est bon) + (-DeltaH R1) (la flèche va dans le sens de la réaction mais comme je l'ai dit plus haut si la flèche est dans ce sens c'est -R1).
Quant tu fais ton diagramme de Hess tu as deux possibilités:
* soit tu met toutes tes fleches allant vers le produit de la réaction (donc celle de gauche qui descend et celle de droite qui remonte): dans ce cas il faut que tu fasse en notant à coté au signe de tes enthalpies. Mais quand tu passe au calcul tu n'a plus qu'à faire l'enthalpie de réaction = la somme des enthalpies de ton autre chemin (car toutes tes flèches seront dans le bon sens)
* soit tu met les flèches dans le sens des enthalpies qu'on te donne dans l'énoncé donc tu n'as pas de changement de signe à faire sur ton diagramme. Mais attention au moment de passer au calcul il faut bien que tu aille dans le sens de la réaction (ici vers la formation de CO2 et H2O qui sont les produit de la réaction du propane).
Tu as compris ?


La Gueuse- Messages : 293
Date d'inscription : 07/12/2014
 QCM 28 TK2
QCM 28 TK2
Oui merci beaucoup pour ta réponse ça m'a tellement éclairée car je faisais un gros mélange de tout ! 
V.Dsw- Messages : 91
Date d'inscription : 10/09/2016
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des Talc-Khôlles (TK) et des tutorats :: CHIMIE GENERALE :: TK & Tutos 2015-2016
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum