Exercice d'application oxydo-réduction
2 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE GENERALE
Page 1 sur 1
 Exercice d'application oxydo-réduction
Exercice d'application oxydo-réduction
Bonjour j'ai deux questions concernant deux exercices différents
Tout d'abord par rapport à l'équilibre de cette équation : Pourquoi l'on ajoute 5charges négatives et non pas 4 (3 charges négatives et 1 charge positive) et aussi pouvons nous mettre le nombre stoechiométrique 2 devant le Br qui se retrouve dans les réactifs à la place de mettre 1/2 devant le Br des produits afin d'annuler les charges ?
BrO3-(aq) / Br2(aq)
BrO3- + 6H+ + 5e- = 1/2Br2 + 3H2O
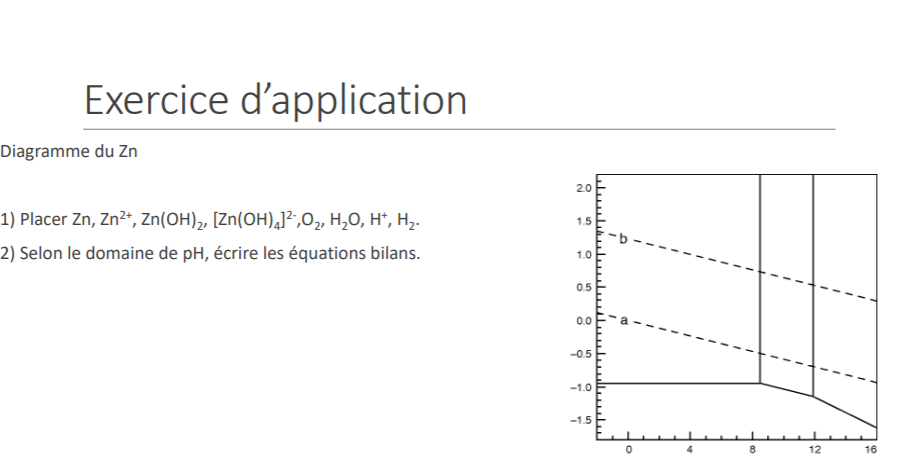
Et seconde question concernant cet exercice d'application : je ne comprends par très bien la question 2, comment à partir du diagramme et des données de l'exercice 1 pouvons nous répondre à la question.
Merci d'avance !
Tout d'abord par rapport à l'équilibre de cette équation : Pourquoi l'on ajoute 5charges négatives et non pas 4 (3 charges négatives et 1 charge positive) et aussi pouvons nous mettre le nombre stoechiométrique 2 devant le Br qui se retrouve dans les réactifs à la place de mettre 1/2 devant le Br des produits afin d'annuler les charges ?
BrO3-(aq) / Br2(aq)
BrO3- + 6H+ + 5e- = 1/2Br2 + 3H2O
Et seconde question concernant cet exercice d'application : je ne comprends par très bien la question 2, comment à partir du diagramme et des données de l'exercice 1 pouvons nous répondre à la question.

Merci d'avance !
paolaaa- Messages : 129
Date d'inscription : 06/11/2020
 Re: Exercice d'application oxydo-réduction
Re: Exercice d'application oxydo-réduction
Salut !
1. À gauche de l'équation, on a : du BrO3⁻, avec 1 charge négative, du H+ et des électrons
À droite de l'équation, on a : du Br2 et de l'H2O, tous deux électriquement neutres.
il faut donc équilibrer l'équation de sorte à ce qu'il y ait :
- La même quantité de chaque atome de part et d'autre de ton égal
- La même quantité totale de charge (donc ici puisque la somme des charges est de 0 à droite, elle doit être de 0 à gauche également
Donc dans un premier temps, on équilibre les atomes :
Tu mets 1/2 devant Br2 pour avoir 1 Br de chaque côté
Tu multiplies H2O par 3 pour avoir 3 O de chaque côté
Tu ajoutes des H+ à gauche pour qu'il y autant de H de chaque côté : 2 × 3 = 6 H à droite, donc 6 H+
Les atomes sont équilibrés, donc maintenant on s'intéresse aux charges:
Au total à gauche on a 1 charge nég portée par le BrO3⁻ et 6 charges positives via les H+
La somme est donc de +5, donc il faut ajouter 5 charges négatives pour les neutraliser : on met donc 5 électrons
On a donc bien au final électroneutralité de part et d'autre du égal
2. Une fois que tu as placé les espèces sur le diagramme, tu peux déterminer le couple ox/réd et le couple acide/base et donc établir les équations ox/réd et acide/base !
Est-ce que c'est plus clair pour toi ?
1. À gauche de l'équation, on a : du BrO3⁻, avec 1 charge négative, du H+ et des électrons
À droite de l'équation, on a : du Br2 et de l'H2O, tous deux électriquement neutres.
il faut donc équilibrer l'équation de sorte à ce qu'il y ait :
- La même quantité de chaque atome de part et d'autre de ton égal
- La même quantité totale de charge (donc ici puisque la somme des charges est de 0 à droite, elle doit être de 0 à gauche également
Donc dans un premier temps, on équilibre les atomes :
Tu mets 1/2 devant Br2 pour avoir 1 Br de chaque côté
Tu multiplies H2O par 3 pour avoir 3 O de chaque côté
Tu ajoutes des H+ à gauche pour qu'il y autant de H de chaque côté : 2 × 3 = 6 H à droite, donc 6 H+
Les atomes sont équilibrés, donc maintenant on s'intéresse aux charges:
Au total à gauche on a 1 charge nég portée par le BrO3⁻ et 6 charges positives via les H+
La somme est donc de +5, donc il faut ajouter 5 charges négatives pour les neutraliser : on met donc 5 électrons
On a donc bien au final électroneutralité de part et d'autre du égal
2. Une fois que tu as placé les espèces sur le diagramme, tu peux déterminer le couple ox/réd et le couple acide/base et donc établir les équations ox/réd et acide/base !
Est-ce que c'est plus clair pour toi ?

Asticoo- Messages : 589
Date d'inscription : 22/09/2017
 Exercice d'application oxydo-réduction
Exercice d'application oxydo-réduction
Ouii bien plus clair merci !!!
paolaaa- Messages : 129
Date d'inscription : 06/11/2020
 Sujets similaires
Sujets similaires» DS2 Oxydo reduction
» exo 1 cours oxydo-réduction
» Exemple cours Oxydo-réduction
» TK acide-base/oxydo reduction
» Oxydo-reduction potentiel standard et potentiel d'électrode
» exo 1 cours oxydo-réduction
» Exemple cours Oxydo-réduction
» TK acide-base/oxydo reduction
» Oxydo-reduction potentiel standard et potentiel d'électrode
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE GENERALE
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|
