ED UE1 n°2 Ex 6 - Acidité
+7
spounch
Sans-Guillaume
lola
jjj
clo_crbl
Val
.sadek
11 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
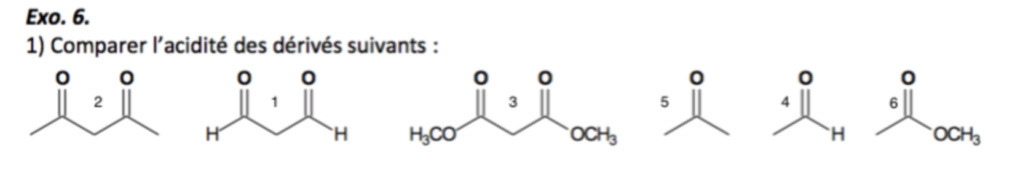
 ED UE1 n°2 Ex 6 - Acidité
ED UE1 n°2 Ex 6 - Acidité
Bonjour,
Concernant la classification des acides il me semble qu'il existe 2 méthodes :
1/ : Regarder la fragilité des liaisons atome-H : + elles sont fragiles + la molécule est acide
2/ : Regarder la base conjuguée de la molécule : + elle est stable + la base est faible donc + l'acide correspondant est fort
Or dans notre ED ci-joint ( https://i.servimg.com/u/f37/19/58/33/76/captur13.png ) le classement (+ acide au - acide) je ne comprends pas pourquoi la 3ème molécule n'est pas devant la n°2, sa base conjugué possède un système conjugué ce qui la rend + faible que la base conjugué de la molécule n°2 celle-ci devrait donc être un acide moins fort que la molécule n°3.
De + dans le chapitre 4 de chimie orga il est dit que les acides carboxyliques sont + acides que les alcools grâce au système conjugué
( https://i.servimg.com/u/f37/19/58/33/76/captur15.png ) , quelle influence a-donc un système conjugué sur l'acidité d'une molécule ? Je suis un peu perdu
Merci à vous.
Concernant la classification des acides il me semble qu'il existe 2 méthodes :
1/ : Regarder la fragilité des liaisons atome-H : + elles sont fragiles + la molécule est acide
2/ : Regarder la base conjuguée de la molécule : + elle est stable + la base est faible donc + l'acide correspondant est fort
Or dans notre ED ci-joint ( https://i.servimg.com/u/f37/19/58/33/76/captur13.png ) le classement (+ acide au - acide) je ne comprends pas pourquoi la 3ème molécule n'est pas devant la n°2, sa base conjugué possède un système conjugué ce qui la rend + faible que la base conjugué de la molécule n°2 celle-ci devrait donc être un acide moins fort que la molécule n°3.
De + dans le chapitre 4 de chimie orga il est dit que les acides carboxyliques sont + acides que les alcools grâce au système conjugué
( https://i.servimg.com/u/f37/19/58/33/76/captur15.png ) , quelle influence a-donc un système conjugué sur l'acidité d'une molécule ? Je suis un peu perdu
Merci à vous.

.sadek- Messages : 46
Date d'inscription : 06/12/2016
Localisation : Namek
Emploi/loisirs : GRAILLE
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Je ne comprend pas non plus ce classement... De la même façon je trouve que la molécule classée en 3 est plus l'acide que la 2, on a un OCH3, donc le CH3 donne, le O aussi du coup mais moins que si il n'y avait que CH3, donc dans la molécule 3 les protons reçoivent moins d'électrons que dans la 2 où les 2 CH3 donnent directement des électrons....
Pourrions avoir une petite explication svp?
Merci !
Pourrions avoir une petite explication svp?
Merci !
Val- Messages : 219
Date d'inscription : 22/10/2016
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Salut !
Je relance ce post parce que je me pose exactement les mêmes questions.
Je viens d'avoir ED et je ne comprends vraiment pas l'ordre qui a été donné (du plus acide au moins acide).
Est-ce que quelqu'un pourrait m'éclairer ?
Merci
P.S : Les molécules sont dans le premier post !
Je relance ce post parce que je me pose exactement les mêmes questions.
Je viens d'avoir ED et je ne comprends vraiment pas l'ordre qui a été donné (du plus acide au moins acide).
Est-ce que quelqu'un pourrait m'éclairer ?
Merci

P.S : Les molécules sont dans le premier post !
clo_crbl- Messages : 59
Date d'inscription : 10/10/2016
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Bonjour,
Je viens d'avoir l'ED aussi et je ne comprends pas le classement non plus
Est ce que quelqu'un pourrait expliquer sil vous plait ?
Merci d'avance
Je viens d'avoir l'ED aussi et je ne comprends pas le classement non plus
Est ce que quelqu'un pourrait expliquer sil vous plait ?
Merci d'avance
jjj- Messages : 116
Date d'inscription : 23/11/2016
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Salut
Je relance une nouvelle fois le topo, j'aimerai bien une petite explication aussi svppp
Je relance une nouvelle fois le topo, j'aimerai bien une petite explication aussi svppp
lola- Messages : 49
Date d'inscription : 15/04/2017
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Salut ! Est e que déjà vous pourriez remettre les images ? Qu'on puissent bien voir.
Ensuite explique bien à quel endroit tu comprend pas. La différence entre quoi et quoi et pourquoi ?
Ca nous aidera pour t'expliquer au mieux.
Bon courage.
Ensuite explique bien à quel endroit tu comprend pas. La différence entre quoi et quoi et pourquoi ?
Ca nous aidera pour t'expliquer au mieux.
Bon courage.
Sans-Guillaume- Messages : 46
Date d'inscription : 25/10/2014
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Bonjour j'ai eu le même ED et je ne comprends pas non plus ce classement, quelqu'un pourrait-il m'aider?
Merci d'avance
PS : les images sont dans le premier post
Merci d'avance
PS : les images sont dans le premier post
Al- Messages : 8
Date d'inscription : 21/11/2017
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
le prof nous a donné (de la plus basique à la plus acide) : 6 < 4 < 5 < 3 < 1 < 2
et je ne comprends pas pourquoi la molécule 1 est plus acide que la molécule 3?
Merci pour la réponse et désolé pour l'attente
et je ne comprends pas pourquoi la molécule 1 est plus acide que la molécule 3?
Merci pour la réponse et désolé pour l'attente
Al- Messages : 8
Date d'inscription : 21/11/2017
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Coucou,
Dans ta molécule 3, le système conjugué comprend la fonction carbonyle et le O porteur de ton méthyl. Comme c'est une mise en commun d'électrons, l'effet attracteur est moindre : le O lié au carbone (porteur du H) met déjà ses électrons en commun donc est moins attracteur.
De plus, dans ta molécule 1, le H est directement porté par le C qui porte la fonction carbonyle (effet attracteur très fort) alors que dans la molécule 3, le carbone qui porte le H est lié d'abord par une simple liaison au O (effet attracteur moins fort).
J'espère avoir été claire Par écrit ce n'est pas évident
Par écrit ce n'est pas évident 
Sinon tu peux aussi regarder la base conjuguée et comparer leur stabilité !
Bon courage
Dans ta molécule 3, le système conjugué comprend la fonction carbonyle et le O porteur de ton méthyl. Comme c'est une mise en commun d'électrons, l'effet attracteur est moindre : le O lié au carbone (porteur du H) met déjà ses électrons en commun donc est moins attracteur.
De plus, dans ta molécule 1, le H est directement porté par le C qui porte la fonction carbonyle (effet attracteur très fort) alors que dans la molécule 3, le carbone qui porte le H est lié d'abord par une simple liaison au O (effet attracteur moins fort).
J'espère avoir été claire
Sinon tu peux aussi regarder la base conjuguée et comparer leur stabilité !
Bon courage
Wendy99- Messages : 94
Date d'inscription : 27/09/2018
 acidité
acidité
Bonjour,
Je ne comprends pas comment déprotoner pour regarder la stabilité de la base conjuguée car avec un acide carboxilique on enlève le H du -OH mais ici il ny a pas de fonction OH donc quel H faut-il regarder?
Pour les molécules 3 et 6, le O lié à CH3 n'exerce pas plutot un effet attracteur -I et -M?
De plus, pour cet ED MR Michon ne m'a pas donné le même classement, il a donné celui ci : (de la plus basique à la plus acide ) : 6<5<4<3<2<1
Quel est alors le bon classement?
Merci d'avance
Je ne comprends pas comment déprotoner pour regarder la stabilité de la base conjuguée car avec un acide carboxilique on enlève le H du -OH mais ici il ny a pas de fonction OH donc quel H faut-il regarder?
Pour les molécules 3 et 6, le O lié à CH3 n'exerce pas plutot un effet attracteur -I et -M?
De plus, pour cet ED MR Michon ne m'a pas donné le même classement, il a donné celui ci : (de la plus basique à la plus acide ) : 6<5<4<3<2<1
Quel est alors le bon classement?
Merci d'avance
marie2018- Messages : 297
Date d'inscription : 03/10/2018
 Re: ED UE1 n°2 Ex 6 - Acidité
Re: ED UE1 n°2 Ex 6 - Acidité
Salut,
Alors le bon classement c'est celui qui est donné sur l'image (du plus acide au moins acide). L'ordre de Michon est le même sauf qu'il par du moins au plus acide.
Ici comme tu n'as pas de liaison O-H tu es obligé de déprotoné un carbone et donc ton acidité se trouvera sur une liaison C-H.
Le O exerce bien un effet I- et une fois le carbone déprotoné il est inclue dans le système mésomère et alors le O a une effet M+.
Bon courage
Alors le bon classement c'est celui qui est donné sur l'image (du plus acide au moins acide). L'ordre de Michon est le même sauf qu'il par du moins au plus acide.
Ici comme tu n'as pas de liaison O-H tu es obligé de déprotoné un carbone et donc ton acidité se trouvera sur une liaison C-H.
Le O exerce bien un effet I- et une fois le carbone déprotoné il est inclue dans le système mésomère et alors le O a une effet M+.
Bon courage
Lenouch- Messages : 136
Date d'inscription : 07/02/2017
Age : 26
 Sujets similaires
Sujets similaires» ED 2, exo 6 acidité
» Classement des acidités
» Comparer acidité
» acidité et basicité
» Acidité molécule
» Classement des acidités
» Comparer acidité
» acidité et basicité
» Acidité molécule
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum