règle de l'octet
3 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des colles :: Très très ancien
Page 1 sur 1
 règle de l'octet
règle de l'octet
Salut !
Dans une question de décembre 2005 Boury demande parmi différentes molécules, lesquelles obéissent à la règle de l'octet.
Dans ces molécules il y a H2O2. Pouvez vous confirmer qu'on ne la coche pas, puisqu'elle obéit à la règle du duet ?
Et dans ce même concours, je ne suis pas sûre de moi pour la figure de répulsion et la géométrie de NO3-...
Si je fais la méthode bidouille j'ai 32 électrons /8 = 4, donc AX4; mais ça ne me praâit pas logique... et si je réfléchis avec Lewis je ne sais pas trop quoi faire du doublet non liant sur le O...
Pouvez vous m'éclairer ?
Merci d'avance !
Dans une question de décembre 2005 Boury demande parmi différentes molécules, lesquelles obéissent à la règle de l'octet.
Dans ces molécules il y a H2O2. Pouvez vous confirmer qu'on ne la coche pas, puisqu'elle obéit à la règle du duet ?
Et dans ce même concours, je ne suis pas sûre de moi pour la figure de répulsion et la géométrie de NO3-...
Si je fais la méthode bidouille j'ai 32 électrons /8 = 4, donc AX4; mais ça ne me praâit pas logique... et si je réfléchis avec Lewis je ne sais pas trop quoi faire du doublet non liant sur le O...
Pouvez vous m'éclairer ?
Merci d'avance !
Marion Mllrd- Messages : 83
Date d'inscription : 05/09/2016
 Re: règle de l'octet
Re: règle de l'octet
Coucou,
Alors ta molécule d'H2O2 respecte bien la règle de l'octet. Je te met une image de la molécule
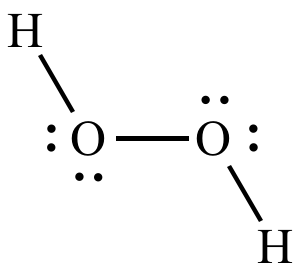
Les 2 oxygènes ont bien 8 électrons autour d'eux (en comptant les liaisons) et les H en ont bien 2.
Pour la molécule de NO3- attention dans ton calcul:
24/8 = 3 donc tu obtiens AX3.
En fait la molécule de NO3- est pas facile à trouver il s'agit de celle la :
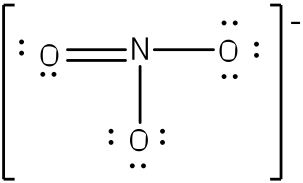
Tu n'as pas de doublets autour du N, la charge négative vient du fait que le N à un électron en moins donc il est chargé positivement et 2 oxygène ont un électron en plus donc ils sont chargés négativement , la résultante fais que la molécule est chargée -1.
Est ce plus clair ?
Bon courage
Alors ta molécule d'H2O2 respecte bien la règle de l'octet. Je te met une image de la molécule

Les 2 oxygènes ont bien 8 électrons autour d'eux (en comptant les liaisons) et les H en ont bien 2.
Pour la molécule de NO3- attention dans ton calcul:
Nb d'électrons de valence pour le O : 6 donc 6 x 3 = 18
Nb d'électrons de valence du N : 5
On compte 1 électron en plus à cause de la charge -
Donc au total : 18 + 5 + 1 = 24
Nb d'électrons de valence du N : 5
On compte 1 électron en plus à cause de la charge -
Donc au total : 18 + 5 + 1 = 24
24/8 = 3 donc tu obtiens AX3.
En fait la molécule de NO3- est pas facile à trouver il s'agit de celle la :

Tu n'as pas de doublets autour du N, la charge négative vient du fait que le N à un électron en moins donc il est chargé positivement et 2 oxygène ont un électron en plus donc ils sont chargés négativement , la résultante fais que la molécule est chargée -1.
Est ce plus clair ?
Bon courage

La Gueuse- Messages : 293
Date d'inscription : 07/12/2014
 Re: règle de l'octet
Re: règle de l'octet
Beaucoup plus clair, merci beaucoup ! et bravo pour la rapidité !
Marion Mllrd- Messages : 83
Date d'inscription : 05/09/2016
 Re: règle de l'octet
Re: règle de l'octet
bonjour
est ce que NO2 respecte la règle de l'octet
J'ai fais : N(5e de valence)
O (6electrons de valences)
5+6x2 = 17
Donc je trouve 2 liaisons
Un reste de 1 (que je divise par 2 et donc = 0,5 = 1 doublet non liant)
Ducoup N a deux liaisons et un doublet mais ducoup pour ça respecte pas la règle de l'octet mais ça me semble bizarre
Je sais pas si je procède correctement…

est ce que NO2 respecte la règle de l'octet
J'ai fais : N(5e de valence)
O (6electrons de valences)
5+6x2 = 17
Donc je trouve 2 liaisons
Un reste de 1 (que je divise par 2 et donc = 0,5 = 1 doublet non liant)
Ducoup N a deux liaisons et un doublet mais ducoup pour ça respecte pas la règle de l'octet mais ça me semble bizarre
Je sais pas si je procède correctement…
jjj- Messages : 116
Date d'inscription : 23/11/2016
 Re: règle de l'octet
Re: règle de l'octet
Coucou,
La molécule de NO2 est un peu particulière.
Attention, Certes si dans ta division euclidienne tu as un 0,5 on vous a dit de mettre 1 il faut garder à l'esprit qu'il s'agit d'un électron célibataire et non d'un DNL.
Quand tu dessine ta molécule de NO2 la première molécule qu'on aurait tendance à faire c'est un N faisant 2 double liaisons avec les O et son électron célibataire. Cependant cette représentation est fausse car ne respecte pas l'octet (le N aurait plus de 8 e- autour de lui ce qui n'est pas possible). Donc en fait l'électron célibataire est délocalisé sur un O comme ceci:
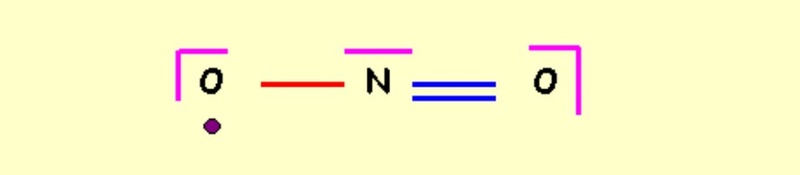
J'espère que c est clair.
Bon courage
La molécule de NO2 est un peu particulière.
Attention, Certes si dans ta division euclidienne tu as un 0,5 on vous a dit de mettre 1 il faut garder à l'esprit qu'il s'agit d'un électron célibataire et non d'un DNL.
Quand tu dessine ta molécule de NO2 la première molécule qu'on aurait tendance à faire c'est un N faisant 2 double liaisons avec les O et son électron célibataire. Cependant cette représentation est fausse car ne respecte pas l'octet (le N aurait plus de 8 e- autour de lui ce qui n'est pas possible). Donc en fait l'électron célibataire est délocalisé sur un O comme ceci:

J'espère que c est clair.
Bon courage

La Gueuse- Messages : 293
Date d'inscription : 07/12/2014
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des colles :: Très très ancien
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum