EXOS CHAPITRE 3
2 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
 EXOS CHAPITRE 3
EXOS CHAPITRE 3
Salut,
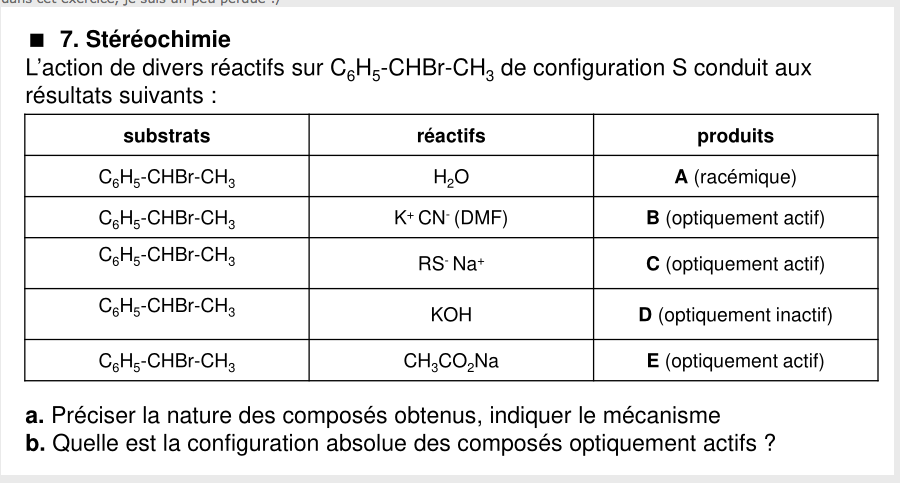
Je reviens sur ce post, comment peut on savoir que RS-NA+ pour la proposition C est un solvant aprotique .. ??
..
https://talc.forumgratuit.org/t6877-exercice-7-poly-3-gautret
En fait pourriez vous me dire quels seraient les mécanismes qui aboutissent à avoir un composé "actif" svp ?
(j'ai fais ma propre liste je ne sais pas si cela est bon ..)
pour moi cela serait :
optiquement actif = SN2
racémique = SN1
optiquement inactif = E1 et E2 car formation d'un alcène
Pourriez vous me dire si stéréospécifique = actif ? et m'expliquer cette notion concrètement ?
MERCI !
Je reviens sur ce post, comment peut on savoir que RS-NA+ pour la proposition C est un solvant aprotique .. ??
..
https://talc.forumgratuit.org/t6877-exercice-7-poly-3-gautret
En fait pourriez vous me dire quels seraient les mécanismes qui aboutissent à avoir un composé "actif" svp ?
(j'ai fais ma propre liste je ne sais pas si cela est bon ..)
pour moi cela serait :
optiquement actif = SN2
racémique = SN1
optiquement inactif = E1 et E2 car formation d'un alcène
Pourriez vous me dire si stéréospécifique = actif ? et m'expliquer cette notion concrètement ?

MERCI !
Tia- Messages : 177
Date d'inscription : 16/10/2017
 Re: EXOS CHAPITRE 3
Re: EXOS CHAPITRE 3
Salut !
Un solvant aprotique est un solvant dépourvu de protons H+. Ici RS-NA+ ne possède pas d'hydrogène et ne peux donc pas libérer de protons, c'est donc un solvant aprotique (à l'inverse, H2O est un solvant protique puisque susceptible de libérer des H+)
SN1 donne un mélange racémique, c'est-à-dire que l'on va trouver 2 énantiomères en quantité équimolaire.
Si la molécule initiale possède 4 substituants différents, elle a donc un carbone asymétrique et sera par conséquent optiquement active.
Elle donnera alors 2 énantiomères images l'un de l'autre, qui seront eux aussi optiquement actifs.
Cependant comme on aura 2 énantiomères d'activité optique opposée en quantité égale, le mélange sera optiquement inactif (l'activité optique de l'un annule l'activité optique de l'autre).
-> Donc les produits pris individuellement sont optiquement actif, mais le mélange obtenu est optiquement inactif
SN2 est stéréospécifique, ce qui signifie que la fixation du nucléophile ne se fait pas aléatoirement : il n'y a donc qu'un seul produit possible, donc pas de racémisation.
On obtient qu'un seul produit, et si celui-ci possède un carbone asymétrique, il sera optiquement actif.
Pour E1 et E2 effectivement, les réactions aboutissent à la formation d'alcènes, donc pas de carbone asymétrique, donc pas d'activité optique.
Stéréospécifique ne veut pas nécessairement optiquement actif !
La stéréospécificité qualifie une réaction pour laquelle il va y avoir un "endroit" où se fixer pour le substituant qui arrive : par exemple pour SN2, la réaction est dite stéréospécifique parce que le nucléophile doit se fixer du côté opposé à celui où est fixé l'halogène.
Le caractère optiquement actif/inactif d'une molécule est lié à la présence ou non d'un carbone asymétrique. Si on a un carbone asymétrique, la molécule est optiquement active, sinon elle est optiquement inactive.
Du coup, tout ce qu'on a dit plus haut n'est évidemment vrai que dans le cas où les halogénoalcanes subissant la réaction ont un carbone asymétrique ! (si par exemple tu as un H3-C-X, ce sera optiquement inactif quoi qu'il arrive, puisque sans carbone asymétrique, pas d'activité optique).
Voilà voilà j'espère que ça répond bien à toutes tes questions, et que ça te semble désormais plus clair !
Un solvant aprotique est un solvant dépourvu de protons H+. Ici RS-NA+ ne possède pas d'hydrogène et ne peux donc pas libérer de protons, c'est donc un solvant aprotique (à l'inverse, H2O est un solvant protique puisque susceptible de libérer des H+)
SN1 donne un mélange racémique, c'est-à-dire que l'on va trouver 2 énantiomères en quantité équimolaire.
Si la molécule initiale possède 4 substituants différents, elle a donc un carbone asymétrique et sera par conséquent optiquement active.
Elle donnera alors 2 énantiomères images l'un de l'autre, qui seront eux aussi optiquement actifs.
Cependant comme on aura 2 énantiomères d'activité optique opposée en quantité égale, le mélange sera optiquement inactif (l'activité optique de l'un annule l'activité optique de l'autre).
-> Donc les produits pris individuellement sont optiquement actif, mais le mélange obtenu est optiquement inactif
SN2 est stéréospécifique, ce qui signifie que la fixation du nucléophile ne se fait pas aléatoirement : il n'y a donc qu'un seul produit possible, donc pas de racémisation.
On obtient qu'un seul produit, et si celui-ci possède un carbone asymétrique, il sera optiquement actif.
Pour E1 et E2 effectivement, les réactions aboutissent à la formation d'alcènes, donc pas de carbone asymétrique, donc pas d'activité optique.
Stéréospécifique ne veut pas nécessairement optiquement actif !
La stéréospécificité qualifie une réaction pour laquelle il va y avoir un "endroit" où se fixer pour le substituant qui arrive : par exemple pour SN2, la réaction est dite stéréospécifique parce que le nucléophile doit se fixer du côté opposé à celui où est fixé l'halogène.
Le caractère optiquement actif/inactif d'une molécule est lié à la présence ou non d'un carbone asymétrique. Si on a un carbone asymétrique, la molécule est optiquement active, sinon elle est optiquement inactive.
Du coup, tout ce qu'on a dit plus haut n'est évidemment vrai que dans le cas où les halogénoalcanes subissant la réaction ont un carbone asymétrique ! (si par exemple tu as un H3-C-X, ce sera optiquement inactif quoi qu'il arrive, puisque sans carbone asymétrique, pas d'activité optique).
Voilà voilà j'espère que ça répond bien à toutes tes questions, et que ça te semble désormais plus clair !

Asticoo- Messages : 589
Date d'inscription : 22/09/2017
 Re: EXOS CHAPITRE 3
Re: EXOS CHAPITRE 3
MERCI BCP ! C'est bien plus clair pour moi 
Tia- Messages : 177
Date d'inscription : 16/10/2017
 Sujets similaires
Sujets similaires» Chapitre 3 exercice 13
» chapitre 4 - exemple
» Sur le chapitre 3 de Chimie orga
» Cytokératine chapitre 1 épithélium
» premier chapitre formules des pH
» chapitre 4 - exemple
» Sur le chapitre 3 de Chimie orga
» Cytokératine chapitre 1 épithélium
» premier chapitre formules des pH
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions de cours et d'ED :: CHIMIE ORGANIQUE
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum