QCM 6 -2018
+5
Lutin
marie2018
Brutus
maelle.glb
discodisco
9 participants
Page 1 sur 1
 QCM 6 -2018
QCM 6 -2018
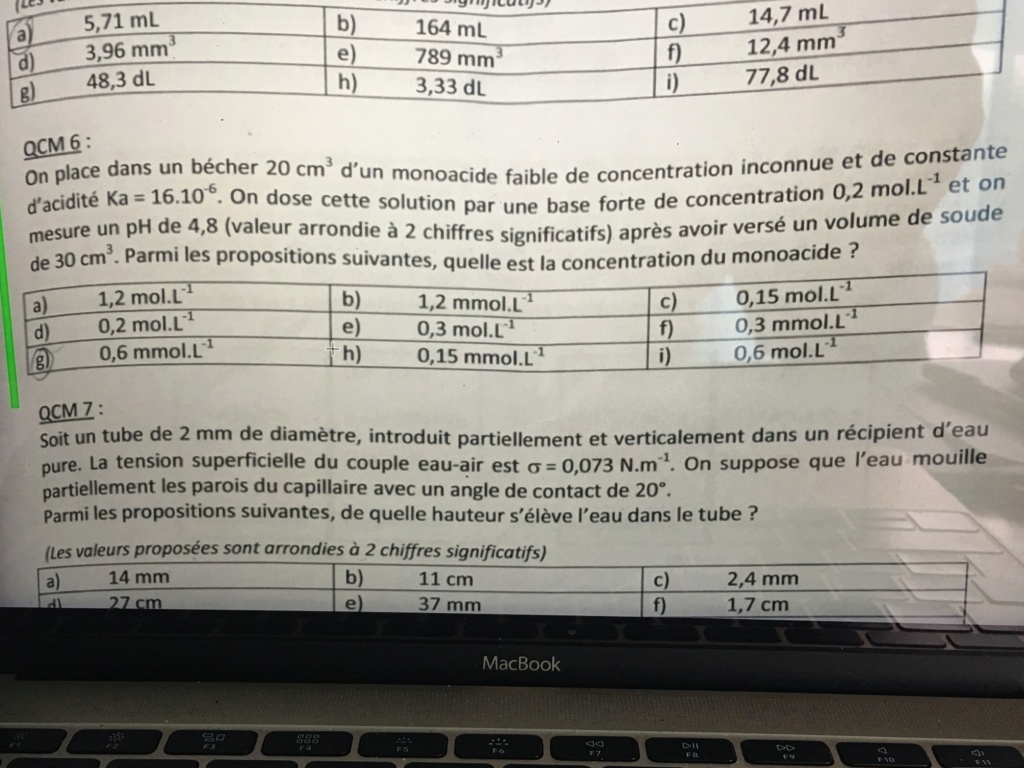
Hello, pour ce qcm je trouve la réponse e) en utilisant la formule du dosage acide faible/ base forte avec un excès de base ? Quelqu'un peut-il confirmer ma réponse car je trouve un peu bizarre que le pH soit égal au pka de l'acide faible sachant qu'il n'y a pas d'équivalence entre les 2 volumes de base et d'acide


discodisco- Messages : 246
Date d'inscription : 17/10/2017
 Re: QCM 6 -2018
Re: QCM 6 -2018
Coucou,
je trouve la même réponse que toi
une confirmation des tuteurs svp?
je trouve la même réponse que toi
une confirmation des tuteurs svp?
maelle.glb- Messages : 19
Date d'inscription : 21/09/2017
 Re: QCM 6 -2018
Re: QCM 6 -2018
Bonjour !
Pour commencer, comment fait-on pour savoir si on est avant, à ou après l'équivalence ? Comme dit plus haut, pKA = pH ici alors que VB n'est pas égal à un demi de Véq, puisqu'on ne connait pas Véq...
Peut-on avoir plus d'indications ?
Merci
Pour commencer, comment fait-on pour savoir si on est avant, à ou après l'équivalence ? Comme dit plus haut, pKA = pH ici alors que VB n'est pas égal à un demi de Véq, puisqu'on ne connait pas Véq...
Peut-on avoir plus d'indications ?
Merci

Brutus- Admin
- Messages : 319
Date d'inscription : 29/11/2017
Age : 24
Localisation : Déni
Emploi/loisirs : Rouler sur les gens
 Re: QCM 6 -2018
Re: QCM 6 -2018
Bonjour,
je me permets de relancer pour savoir si c'est effectivement la e?
merci
je me permets de relancer pour savoir si c'est effectivement la e?
merci
marie2018- Messages : 297
Date d'inscription : 03/10/2018
 Re: QCM 6 -2018
Re: QCM 6 -2018
J'ai une petite interrogation : Pourquoi ce n'est pas plutôt un excès acide ?
Dernière édition par justinbl le Mer 1 Mai - 19:11, édité 1 fois
justinbl- Admin
- Messages : 96
Date d'inscription : 17/09/2018
Localisation : At Ohm
 Re: QCM 6 -2018
Re: QCM 6 -2018
J'ai une petite interrogation : Pourquoi ce n'est pas plutôt un excès acide ?
En effet, si nous calculons la valeur du pKa on trouve que pH = pKa ( pKa = - log 10^-6 = 4,8 ) ce qui veut dire que nous sommes à la demi éqivalence et on n'a pas encore dépassé le point d'équivalence.
Ne devons nous pas ds ce cas utiliser la formule d'exces d'acide ?
merci d'avance
justinbl- Admin
- Messages : 96
Date d'inscription : 17/09/2018
Localisation : At Ohm
 Re: QCM 6 -2018
Re: QCM 6 -2018
Bonjour !
je me permets de relancer, mais comment fait-on pour savoir si on est en excès d'acide ou de base (pas que pour cette question mais en général) ? désolé pour la question bête mais j'ai du mal avec ça
je me permets de relancer, mais comment fait-on pour savoir si on est en excès d'acide ou de base (pas que pour cette question mais en général) ? désolé pour la question bête mais j'ai du mal avec ça
Guest- Invité
 Re: QCM 6 -2018
Re: QCM 6 -2018
En fonction de l'évolution de ton pH et de ton pKa : si pH = pKa alors on est à l'équilibre, si pH < pKa on est en excès d'acide et si pH > pKa = excès de base
Bon courage bisous
Bon courage bisous
ChloéJ- Messages : 46
Date d'inscription : 03/11/2017
 Re: QCM 6 -2018
Re: QCM 6 -2018
excusez moi d'encore relancer le sujet, mais je ne comprends pas pourquoi au lieu de faire ça, on ne part simplement pas du fait que comme on est à demi équivalence : CbVb=CAVA/2 et ensuite on isole CA, avec cette méthode pour moi c'est la D qui est bonne :/

Aristocrate- Messages : 77
Date d'inscription : 07/10/2018
Age : 24
Localisation : Kviland
Emploi/loisirs : Dormir
 Re: QCM 6 -2018
Re: QCM 6 -2018
Saluut
Je suis d'accord avec toi concernant la méthode, à demi-équivalence on a bien Cb.Vb=(Ca.Va)/2 soit Ca=2Cb.Vb/Va
Comme 1cm3=1mL
AN : Ca= 2x0,2x30/20 = 0,6 mol.L-1
Et c'est bien la réponse I
Si c'est toujours pas clair pour toi montre-moi ton raisonnement pour que je te dise ce qui coince
Je suis d'accord avec toi concernant la méthode, à demi-équivalence on a bien Cb.Vb=(Ca.Va)/2 soit Ca=2Cb.Vb/Va
Comme 1cm3=1mL
AN : Ca= 2x0,2x30/20 = 0,6 mol.L-1
Et c'est bien la réponse I
Si c'est toujours pas clair pour toi montre-moi ton raisonnement pour que je te dise ce qui coince
auvray.anais- Messages : 159
Date d'inscription : 23/09/2018
Age : 23
 Re: QCM 6 -2018
Re: QCM 6 -2018
auvray a écrit:Saluut
Je suis d'accord avec toi concernant la méthode, à demi-équivalence on a bien Cb.Vb=(Ca.Va)/2 soit Ca=2Cb.Vb/Va
Comme 1cm3=1mL
AN : Ca= 2x0,2x30/20 = 0,6 mol.L-1
Et c'est bien la réponse I
Si c'est toujours pas clair pour toi montre-moi ton raisonnement pour que je te dise ce qui coince
ça ratais parce que en VB je mettais le volume total !
Merci !

Aristocrate- Messages : 77
Date d'inscription : 07/10/2018
Age : 24
Localisation : Kviland
Emploi/loisirs : Dormir
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum

