Exercice sur la thermodynamique/thermochimie
2 participants
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des colles :: 2011-2012
Page 1 sur 1
 Re: Exercice sur la thermodynamique/thermochimie
Re: Exercice sur la thermodynamique/thermochimie
Salut !
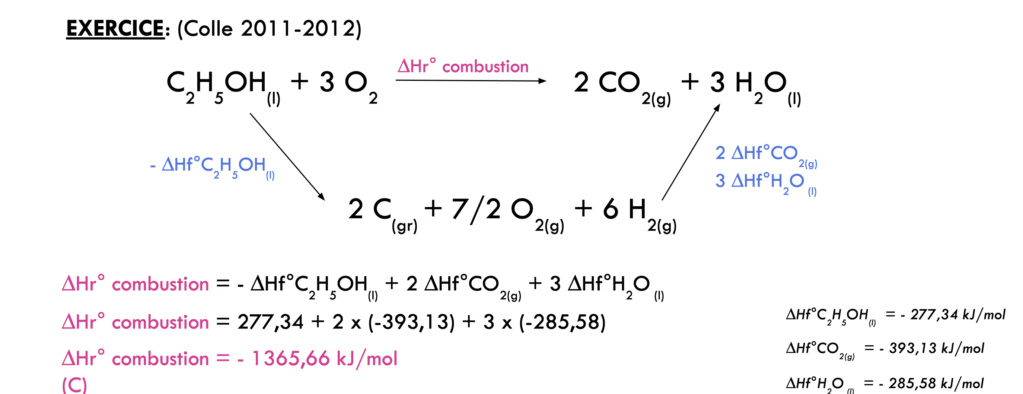
Je pense que tu confonds enthalpie de fusion avec enthalpie de formation. Le delta Hf c’est l’enthalpie de formation de C2H5OH.
Quand tu formes une molécule tu vas libérer de l’énergie mais pour rompre les liaisons au sein d’une molécule et obtenir les corps pur il faut fournir de l’énergie. C’est une réaction endothermique, c’est pour cela que l’enthalpie de dissociation (- delta Hf) de C2H5OH est positive.
J’espère que ça t’aide !
Bon courage
Je pense que tu confonds enthalpie de fusion avec enthalpie de formation. Le delta Hf c’est l’enthalpie de formation de C2H5OH.
Quand tu formes une molécule tu vas libérer de l’énergie mais pour rompre les liaisons au sein d’une molécule et obtenir les corps pur il faut fournir de l’énergie. C’est une réaction endothermique, c’est pour cela que l’enthalpie de dissociation (- delta Hf) de C2H5OH est positive.
J’espère que ça t’aide !
Bon courage

Poussin_L- Messages : 32
Date d'inscription : 12/09/2021
Localisation : Archive of our own
Emploi/loisirs : Trouver des memes de chimie
zoegz aime ce message
 Sujets similaires
Sujets similaires» Exercice d'Application Thermochimie
» THERMODYNAMIQUE
» Thermodynamique
» Thermodynamique
» Exercice 5 poly 2 (Gautret) = exercice 4 ED2 2017-18
» THERMODYNAMIQUE
» Thermodynamique
» Thermodynamique
» Exercice 5 poly 2 (Gautret) = exercice 4 ED2 2017-18
Tutorat Licence Santé Lille Catho :: L1 - Chimie, Chimie Organique, Chimie Structurale, Génétique et Biochimie :: Questions à propos des colles :: 2011-2012
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum