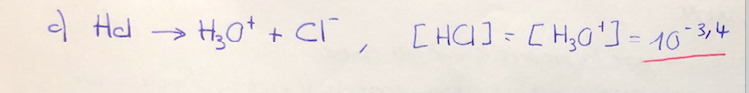UE3B ED1 2019
3 participants
Page 1 sur 1
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
Bonjour !
HCl est un acide fort, donc tu peux l'assimiler à H3O+
Mais, si tu es bien à la question c, HCl n'intervient pas encore. A la question b, tu effectues une dilution. Donc la concentration en H3O+ de la solution diluée sera différente de celle de départ. Tu dois la recalculer pour déterminer le nouveau pH
Bon courage!
HCl est un acide fort, donc tu peux l'assimiler à H3O+
Mais, si tu es bien à la question c, HCl n'intervient pas encore. A la question b, tu effectues une dilution. Donc la concentration en H3O+ de la solution diluée sera différente de celle de départ. Tu dois la recalculer pour déterminer le nouveau pH
Bon courage!
Meisha!- Messages : 6
Date d'inscription : 25/09/2019
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
Salut !
Ce qui te donne cette relation dérive du principe de conservation de la matière.
HCl en se dissociant donne H+ et Cl- (les ions H+ sont assimilés aux ions H3O+) donc on a [HCl]=[H3O+]=[Cl-]
Anaïs
Ce qui te donne cette relation dérive du principe de conservation de la matière.
HCl en se dissociant donne H+ et Cl- (les ions H+ sont assimilés aux ions H3O+) donc on a [HCl]=[H3O+]=[Cl-]
Anaïs
auvray.anais- Messages : 159
Date d'inscription : 23/09/2018
Age : 23
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
J'arrive à comprendre (je crois) comment on arrive à H3O+ = Cl- via l''électroneutralité.
Mais pour la conservation de la matière j'ai :
C0 = HCl + Cl- et donc je vois pas comment H3O+ peut être égal à HCl
et non tout ceci c'est pour la question d)
Mais pour la conservation de la matière j'ai :
C0 = HCl + Cl- et donc je vois pas comment H3O+ peut être égal à HCl
et non tout ceci c'est pour la question d)
Patrick- Messages : 90
Date d'inscription : 01/03/2019
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
Le HCl ou acide chlorhydrique est un acide fort, càd qu'il subit une dissociation totale donc ici, une mole de HCl donne : une mole de H3O+ ET une mole de Cl-
Métaphore peut-être plus parlante, si tu prends un homme et une femme et que tu les fusionnes ca fait UN couple et quand tu les dissocies, ça fait UN homme ET UNE femme, donc on a bien le même nombre stœchiométrique pour : le couple, la femme et l'homme qui est de 1, c'est le même principe pour le HCl
C'est plus clair ?
Métaphore peut-être plus parlante, si tu prends un homme et une femme et que tu les fusionnes ca fait UN couple et quand tu les dissocies, ça fait UN homme ET UNE femme, donc on a bien le même nombre stœchiométrique pour : le couple, la femme et l'homme qui est de 1, c'est le même principe pour le HCl
C'est plus clair ?
auvray.anais- Messages : 159
Date d'inscription : 23/09/2018
Age : 23
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
daac oui je pense ! merci !!!!!
Donc cela fonctionne bien qu'en cas d'acide fort ?
Est ce que cela fonctionne aussi pour une base forte ? ( avec HO- au lieu de H3O+ )
Donc cela fonctionne bien qu'en cas d'acide fort ?
Est ce que cela fonctionne aussi pour une base forte ? ( avec HO- au lieu de H3O+ )
Patrick- Messages : 90
Date d'inscription : 01/03/2019
 Re: UE3B ED1 2019
Re: UE3B ED1 2019
Yes ca fonctionne aussi pour une base forte selon l'équation B+H2O --> BH+ + HO-
(À savoir que pour l'acide fort c'était HCl + H2O aussi dans la première partie de l'équation)
(À savoir que pour l'acide fort c'était HCl + H2O aussi dans la première partie de l'équation)
auvray.anais- Messages : 159
Date d'inscription : 23/09/2018
Age : 23
 Sujets similaires
Sujets similaires» Exo complémentaire TK3 UE3b 2019
» UE3b Ch1 Cavillon
» Q11 TK1 UE3b
» UE3b HbO2H et HBO2
» UE3b Puissance
» UE3b Ch1 Cavillon
» Q11 TK1 UE3b
» UE3b HbO2H et HBO2
» UE3b Puissance
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum